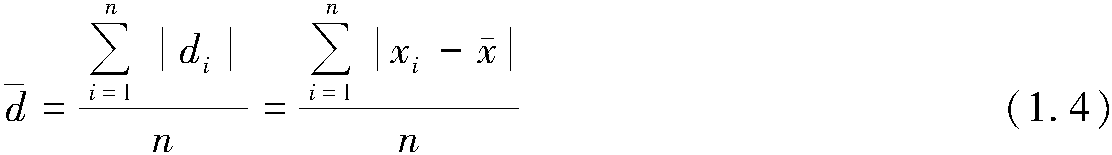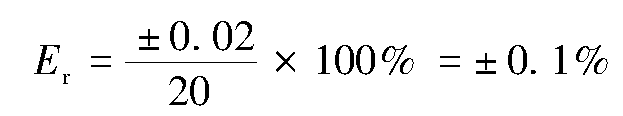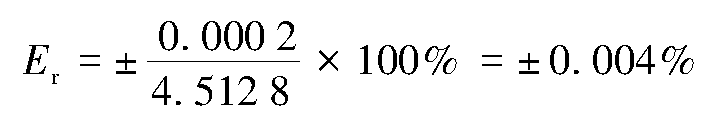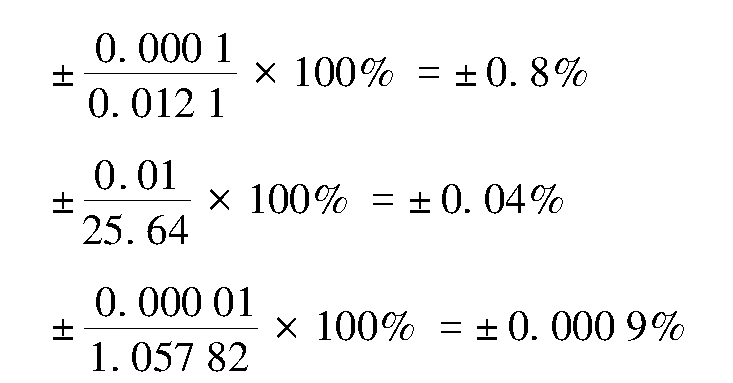1.2.2 有效数字的修约规则
在分析过程中,往往要进行多种不同测量,然后进行运算,得到分析结果。由于各测量值的有效数字位数可能不同,而分析结果却只能含有一位可疑数字,因此要确定各测量值的有效数字位数,将数据后面多余的数字进行取舍,这一过程称为有效数字的修约。
有效数字的修约规则如下:
①四舍六入五成双。
四舍:测量值中被修约数的后面数≤4时,则舍弃。
六入:测量值中被修约数的后面数≥6时,则进位。
五成双:测量值中被修约数的后面数等于5,且5后无数或为0时,若5前面为偶数(0以偶数计),则舍弃;若5前面为奇数,则进1。如果测量值中被修约数的后面数等于5,且5后面还有不为0的任何数时,无 ...... (共844字) [阅读本文]>>

 上一篇
上一篇